5. 衰老
——走向下游
当山不再高耸,水流也就不再湍急。
动物的基因调控网络(gene regulatory network)的两个主要的表观调控机制(即PRC2调控Hox基因簇多米诺式表达,和PRC1调控谱系决定因子基因依次表达)为发育模式提供了固定的框架,对基因调控网络产生滞留机制,使得动物的基因调控网络的等级性(hierarchy)是不可逆的。这两种表观调控机制都具有单一的趋向性:为干细胞提供微环境的成纤维细胞或基质细胞维持Hox基因表达模式,随着年龄的增长,更倾向分化成脂肪细胞;干细胞中PRC1调控谱系决定因子基因依次表达,随着年龄的增长,更倾向表达后期的谱系决定因子基因,使得基因调控网络的等级性的落差变小,干细胞的干性降低。
生命的终点是一束花
–夏加尔
植物没有Hox基因簇,没有PRC1,没有固定的框架和严格意义上的干细胞,基因调控网络的等级性具有可逆性,小分子激素可以使其返回上游状态,只要环境合适,一年生植物只要不开花,植物可以一直活着。
生物虽然会衰老,死亡,但像BBC纪录片《生命的故事》(BBC: life story – parenthood)中所说,“他们最终凭借留下自己的后代,实现某种意义上的不朽(eventually achieve a form of immortality by leaving its own offspring)”。
劳累后的睡眠,暴风后的港口
战乱后的和平,生命后的死亡
让人何其快乐
Sleep after toyle
Port after storm seas
Ease after warre
Death after life
Does greatly please
–埃德蒙.斯宾塞
当波浪意识到自己是水,生死便不再是伤害
–释一行
我和谁都不争,和谁争我都不屑
我爱大自然,其次是艺术
我双手烤着生命之火取暖
火萎了,我也准备走了
I strove with none, for none was worth my strife
Nature I loved, and, next to nature, Art
I warm’d both hands before the fire of life
It sinks, and I am ready to depart
–Walter Savage Landor
我们这一生,爱过,被人爱过,已经是无上的幸运
–George Brickenden & Shirley Brickenden
时光是风
自死亡的方向吹来
–阿多尼斯
分化方向
衰老体现在细胞分化方向的改变,如:骨髓中为造血干细胞提供微环境的成纤维细胞更多向脂肪细胞分化;造血干细胞分化免疫细胞的能力减弱,更多的分化出髓系细胞,如单核细胞,粒细胞,红细胞和血小板;骨骼干细胞分化软骨细胞的能力减弱,更多的向成骨细胞方向分化;毛发干细胞减少毛发方向的分化,更多的分化成毛囊和表皮。分化方向的改变是基因调控网络的等级性和基因被组装成高级结构后所具有的单一趋向性随着时间推移上的一种表现,即随着年龄的增长,细胞更倾向于走向下游的分化命运。
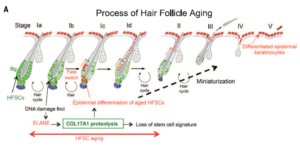 Hair follicle aging is driven by transepidermal elimination of stem cells via COL17A1 proteolysis –Science 351: aad4395 (2016)
Hair follicle aging is driven by transepidermal elimination of stem cells via COL17A1 proteolysis –Science 351: aad4395 (2016)
Morphogenesis and renewal of hair follicles from adult multipotent stem cells –Cell 104: 233 (2001)
Hair follicle stem cell,sebaceous gland stem cell,和interfollicular epidermal stem cell分别是向头发,毛囊和表皮方向分化的前体细胞,它们依次产生。PRC1将谱系决定因子基因组装成染色质高级结构,随着年龄的增长,更倾向于表达位于下游的谱系决定因子,所以形成了青少年一头秀发,中年油腻,老年秃顶的现象。
Let-7,HMGA2
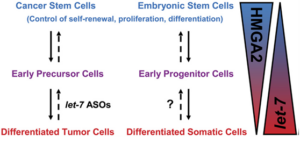 Do cells let-7 determine stemness? –Cell stem cell 2: 8 (2008)
Do cells let-7 determine stemness? –Cell stem cell 2: 8 (2008)
miRNA Let-7和HMGA2(high mobility group AT hook 2)是基因调控网络的组成部分。在发育过程中,随着基因调控网络的等级性走向下游,Let-7和HMGA2也会呈现出趋势化的表达,Let-7随着动物年龄的增长表达逐渐增多,HMGA2则相反。
干细胞与寿命
一些小型动物,例如蠕虫和苍蝇受限于它们的细胞分裂机制,它们体内大部分细胞受损时既不能分裂,也无法被新的细胞取代,因此它们生命衰竭得很快。
Some small animals, like worms and files, are also limited by the mechanisms of their cell division. They’re mostly made up of cells that can’t divide and be replaced when damaged, so their bodies expire more quickly.
–TED-ED 《为什么动物的寿命长短不一 why do animals have such different lifespans》
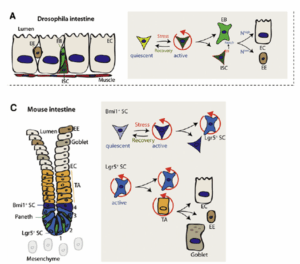
Maintaining tissue homeostasis: dynamic control of somatic stem cell activity –Cell stem cell 9: 402 (2011)
Why climb mount Everest? 为什么要登山
“Because it’s there” 因为山在那里
–Mallory 马洛里
果蝇没有Bmi1基因,只有与之同源的Psc基因,没有shh-Gli1-Bmi1信号途径,也就没有以shh,Bmi1和基因组印记为标志的静态干细胞。小鼠进化出了Bmi1基因,也就有Bmi1决定的静态干细胞。如果把细胞分化过程比喻成高山流水,没有Bmi1,是低海拔的山;进化出Bmi1决定的静态干细胞,就是高海拔的雪山,静态干细胞就像山顶的积雪。有Bmi1决定的静态干细胞,动物获得了更长的寿命,但同时也为癌变埋下伏笔。